√ 価電子数 最外殻電子数 315135-価電子数 最外殻電子数
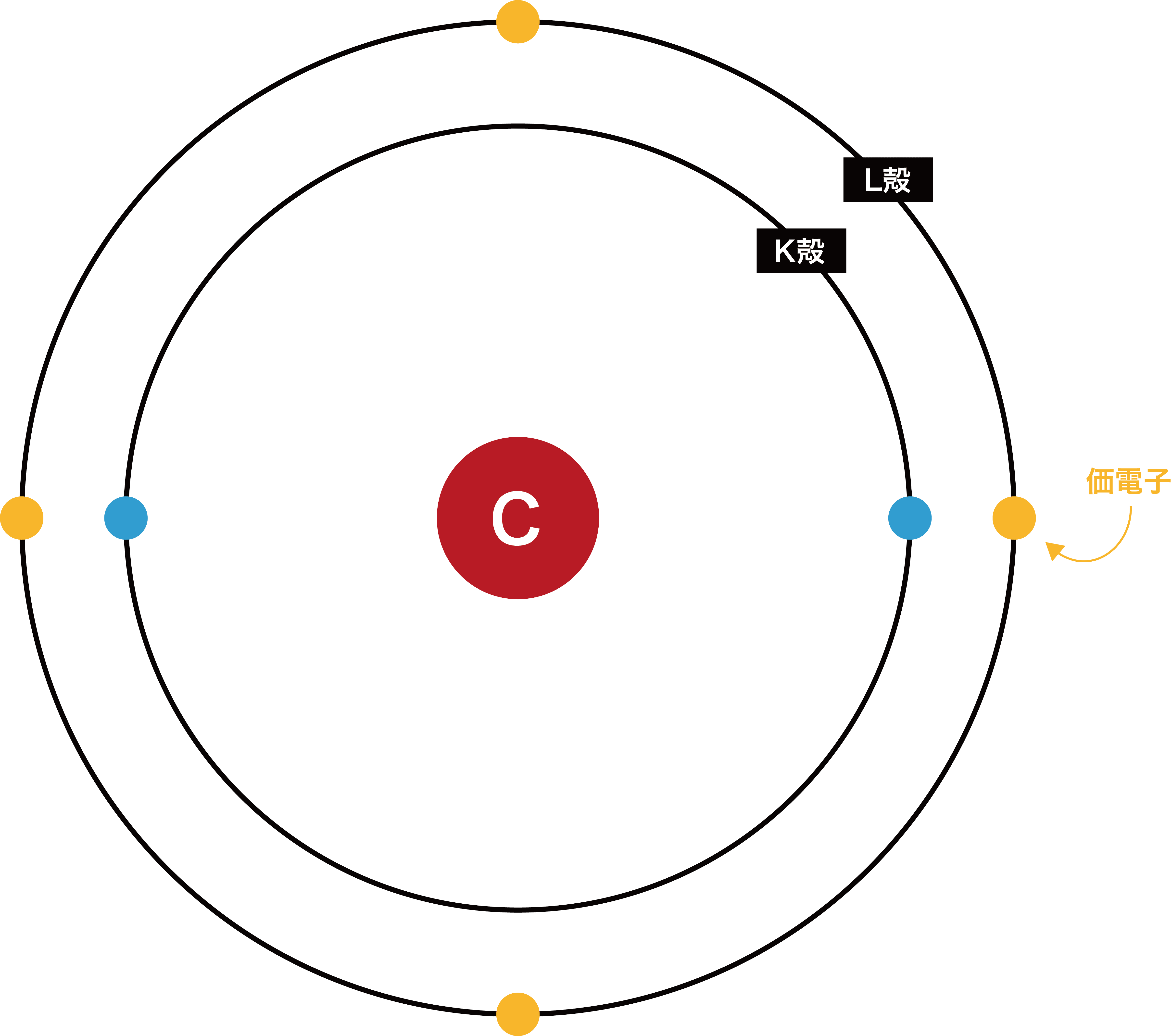
「価電子」 とは、 最外殻にある1から7個の電子 のことです。 「価電子」と「最外殻電子」はよく似ていますが、 「1から7個」 というところが非常に重要です。 今回のCとFの場合は、どちらも「1から7個」の中に収まっています。分子中の原子の「最外殻電子」と「価電子」 分子中の原子について、次のように約束する。 「最外殻電子」:共有している電子を「2個」と数える 「価電子」:共有している電子を「1個」と数える h o h h o h 「最外殻電子」 「価電子」のを( 価電子 )という。最外殻電子の数が1~7個の場合、価電子の数は最外殻電子の数は等しい。 一般に、価電子の数が等しい原子どうしは、よく似た性質を示す。 問2.次の各原子の電子配置を、(例)にならって記せ。また、価電子の数も書け。 K殻 L
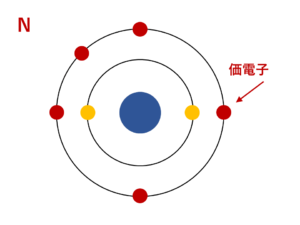
図解 最外殻電子と価電子の定義と違い 結論 希ガスで異なります サイエンスストック 高校化学をアニメーションで理解する
価電子数 最外殻電子数
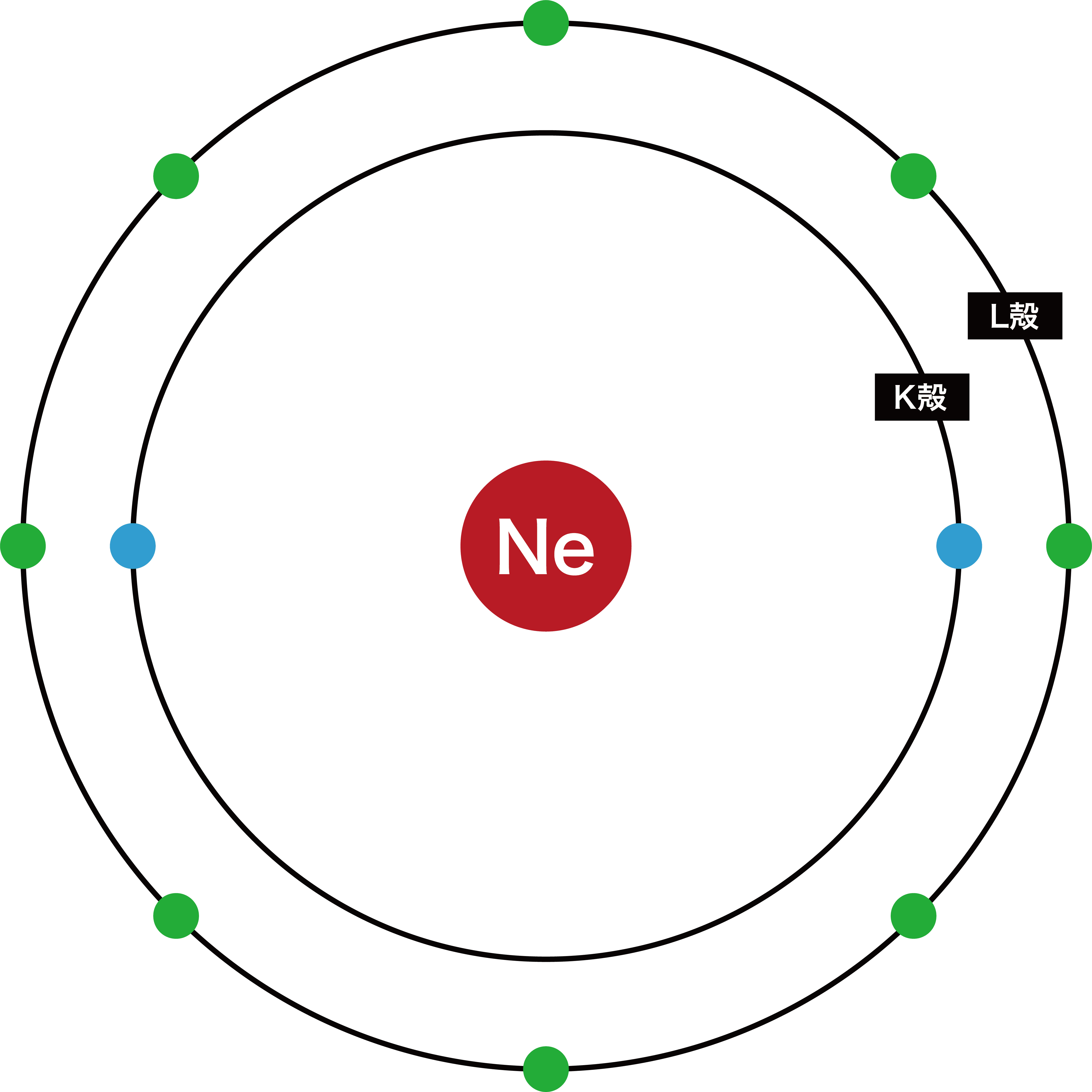
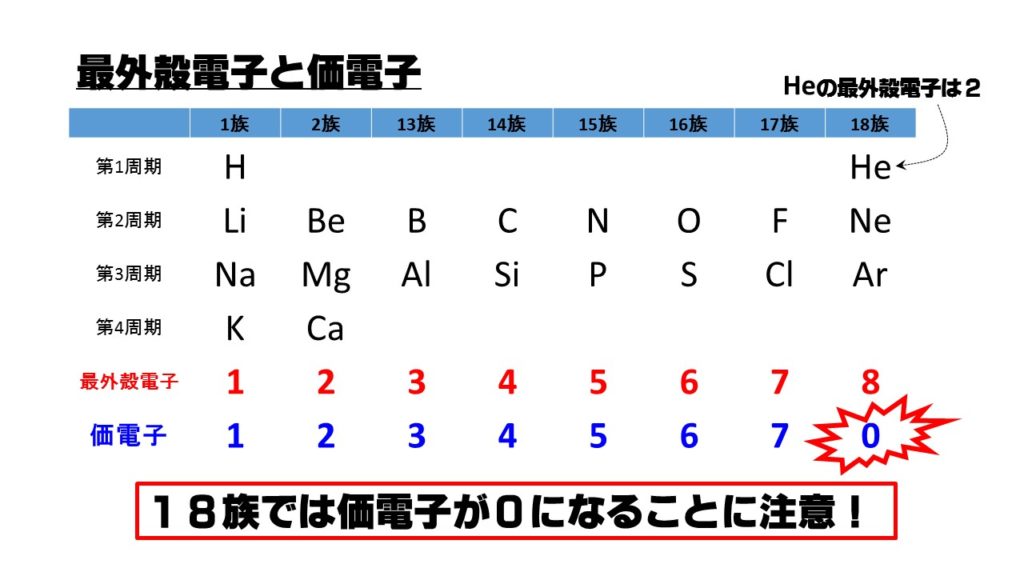
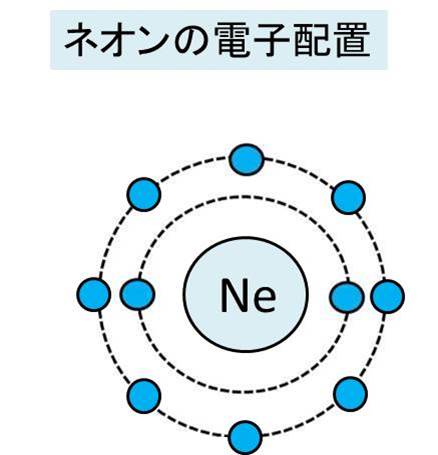
価電子数 最外殻電子数-これらの価電子は、何個になるでしょうか? みなさん、前回の内容を思い出してください。 「価電子」 とは、最外殻にある 1から7個 の電子のことでした。 Neの最外殻電子は8個でしたね。 この場合、価電子の数は何個になるのでしょうか? 答えは、0個です。Aug 05, 17最外殻電子と価電子はほぼイコールであるが、稀に異なる場合がある。 希ガスの一つであるネオンNeは、最外殻電子を「8コ」もっている。 しかし、それら8コの最外殻電子が反応に使われることはほぼないと言っていい。 原子は最外殻が「 希ガスの電子配置 又は オクテット の状態(最外殻電子=8コ)」のときに最も安定となる。 したがって、最外殻電子が既に8
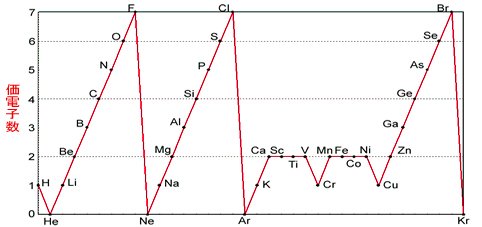



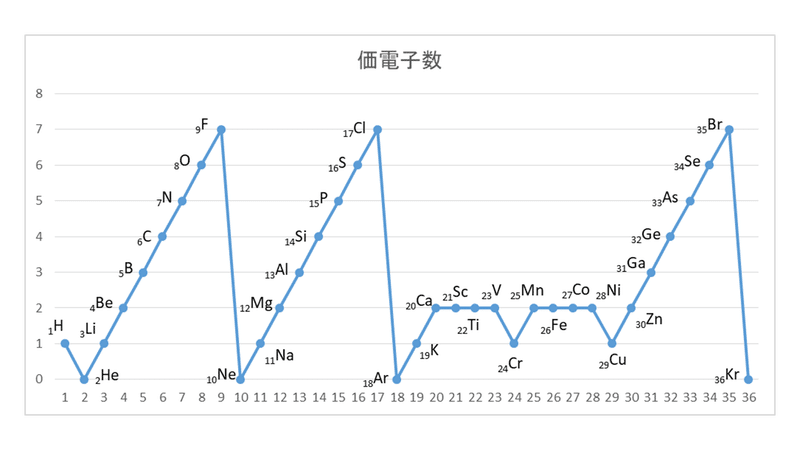
未知なる人間 遥かなる宇宙 Twitter वर 最外殻電子数と価電子数 最外殻電子数とは 単純に最外殻にある電子数です 価電子 とは 反応に関与する電子数です 下図は価電子のグラフです 最外殻電子数のグラフとの違いを考えて下さい T Co
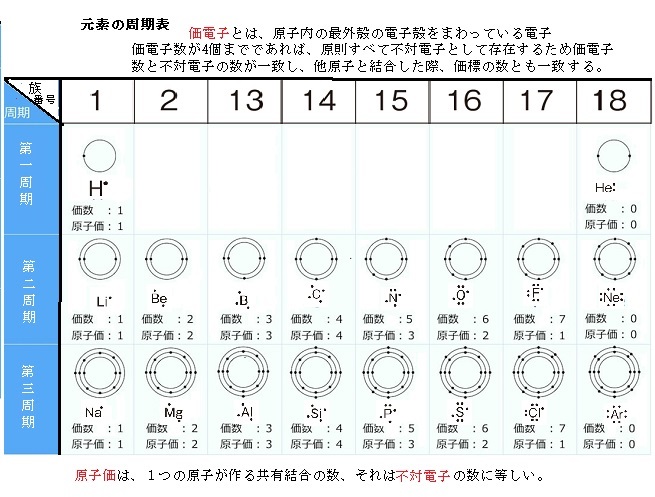
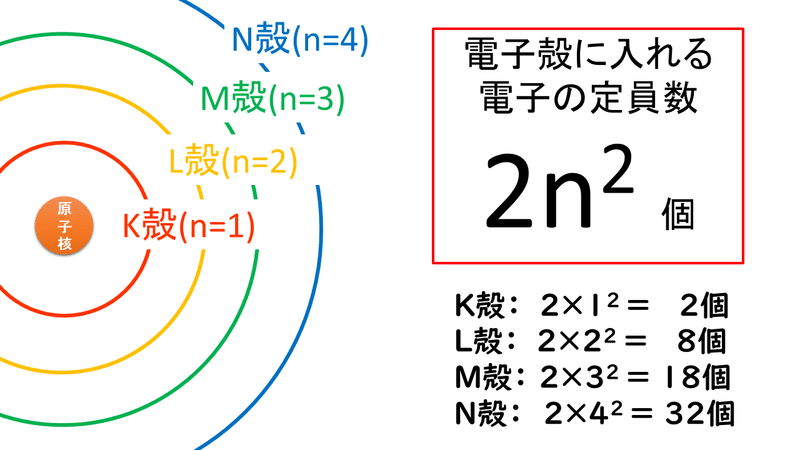
各電子殻に入ることのできる電子の数は主量子数nの関数で 2n 2 である。最も外側の外殻電子を最外殻電子という。電離(イオン化)において失われる電子は、一般には最外殻電子である。価電子は、原子間の化学結合などにおいて重要な役割を果たしていることが多く、物質の性質を特徴づける主要な要素である。 原子価電子 ( げんしかでんし ) ともいう。 基本的に、価電子数は最外殻電子数価電子 ( かでんし 、 ( 英 valence electron )とは、原子内の最外殻の電子殻をまわっている電子のことである。 原子価電子 ( げんしかでんし ) ともいう。 基本的に価電子数は最外殻電子数と等しい。
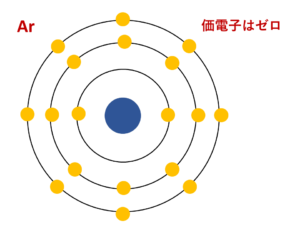
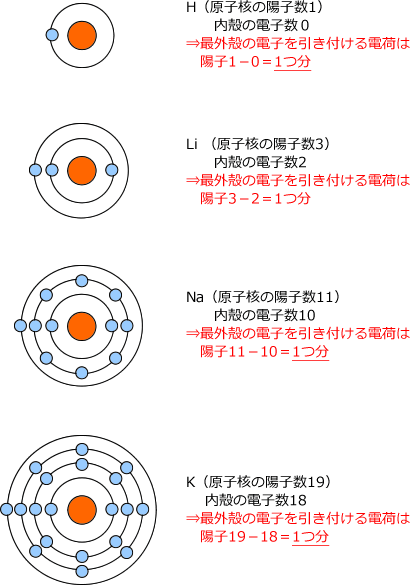
希ガス以外の場合,最外殻電子の数は1~7 個で あり,最外殻電子の数と価電子の数は同じになる。 希ガス の場合は,最外殻電子の数はヘリウムで2 個,それ以外で は8 個であるが,価電子の数は0 とな33 具体例3:スカンジウム21scの電子配置 331 ステップ1:k殻の最大収容数2個を埋める;原子価 (Valence)は、それぞれの原子が他の原子と結びつくときに何本の手を持っているかを示す指数としてイメージできる。 一方、 (原子)価電子 (Valence Electron)は、最外殻にある電子の個数である。
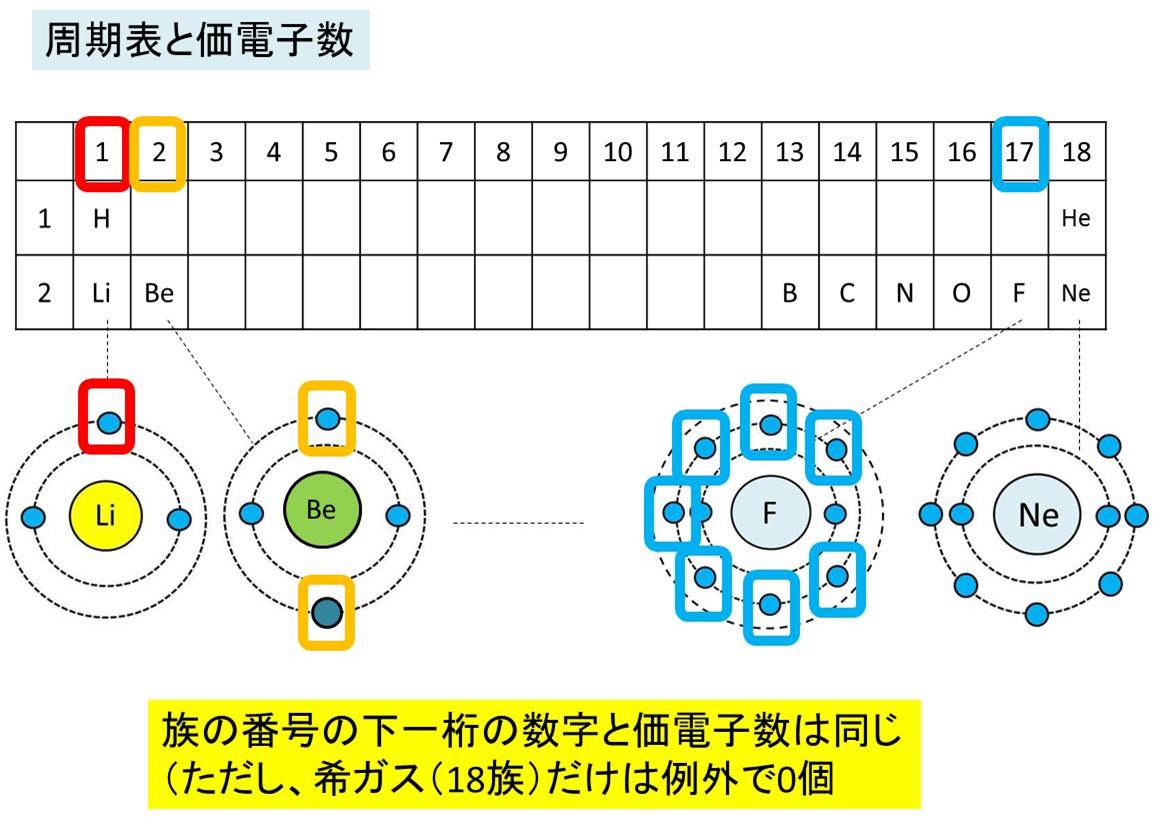
価電子の数は族番号とともに変化し, 同族元素は性質が類似。単体の密度は小さく,化合物は無色のものが多い。 (b) 遷移元素 第4周期以降の3〜11族の元素群。最外殻電子の数は1〜2で,同一 周期でも互いに性質が類似。Sep 13, 123 ステップ3:m殻に最外殻最大収容数8個の電子を埋める;Aug , 価電子とは 基本的には最外殻電子のこと であり、この 価電子の数が同じ原子は化学的性質がよく似ています 。 したがって、先ほど出てきた水素(H)とリチウム(Li)は両方とも価電子が1個なので性質が似ているということになります。



原子とイオン




原子構造と電子配置 価電子 理系ラボ
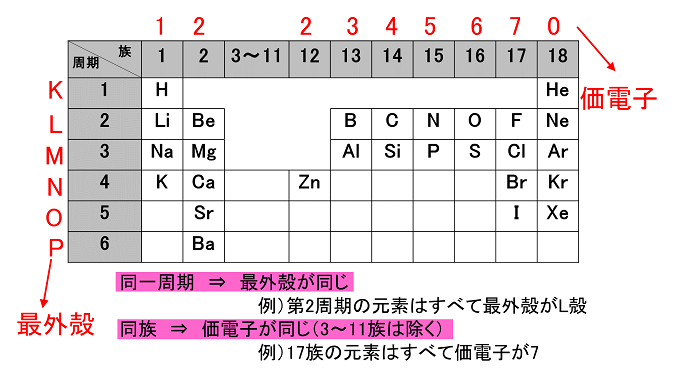
Dec 31, 17価電子の数は希ガスの場合0個、その他の場合は最外殻電子数となる一方、希ガスの最外殻電子数は8個である。つまり価電子と最外殻電子は同義ではない。これは価電子が化学反応に関与できる電子を意味するためだ。 ↑ 2May , 17価電子数の数え方 価電子数を数えたい時は、価電子数が知りたい元素の"族"(周期表のタテのグループ)に注目しよう。 なぜなら、"族"の一の位は、最外殻電子の数(=価電子数)と同じだからだ(例外はあとで説明する)。Oct 04, 12化学 最外殻電子の数 初歩の化学を学習しております。最外殻電子の数は8個までしか入らないそうですが、原子番号21のスカンジウムはM殻に9個入るとテキストに書いてありました。このあたり、理解がイマイ 質問No
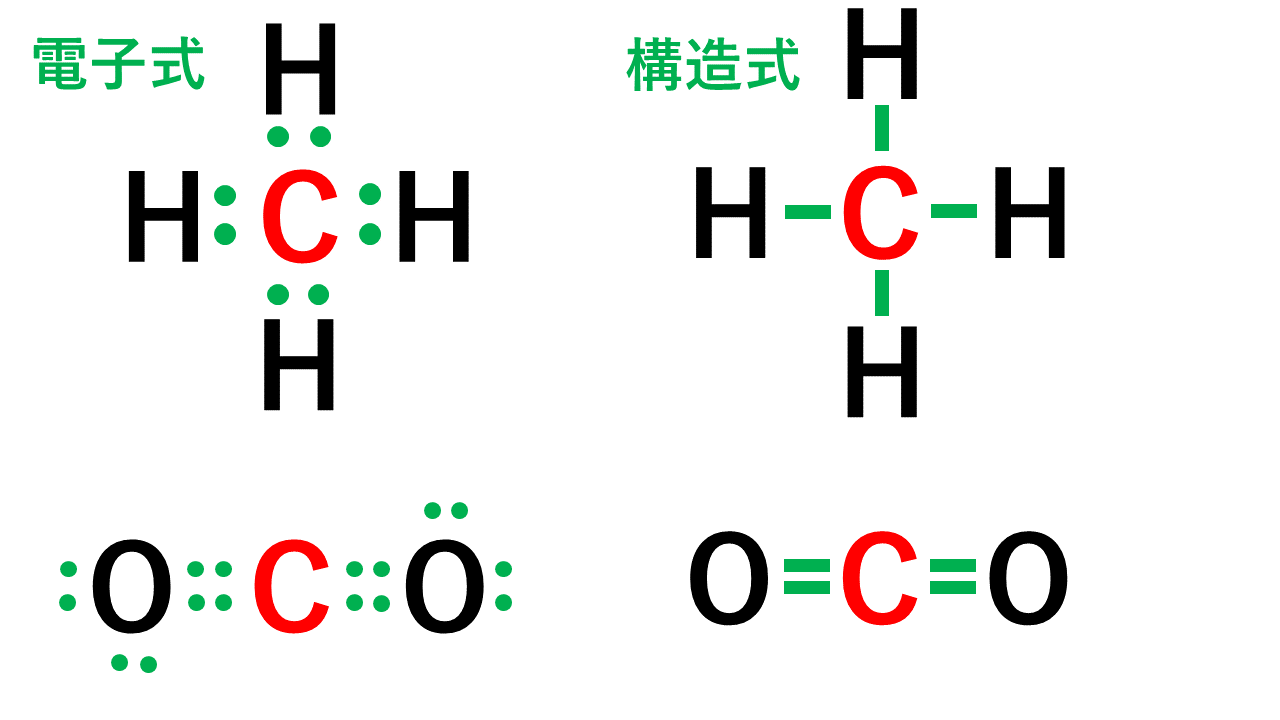



原子価の意味と一覧 価電子 価標の違い Vicolla Magazine



車山高原レア メモリーが語る 元素の周期表
Mar 08, このように、化学変化に関係している最外殻電子のことを、価電子とよんでいます。価電子の数が同じ原子どうしは、化学的性質がよく似ていることが分かっています。 下に示すのは、原子番号1~までの元素の原子の電子配置です。Feb 08, 21極端に言えば「最外殻電子以外の電子は無視しても良い」と言ってもいいかもしれません。 このように化学反応、物質の変化を考える上で重要な最外殻電子の数を「価電子」と呼びます。周期表で同じ族である原子の価電子は同じ値で、例えば炭素やケイ素価電子の説明がよくわかりません。 1行目に「価電子が同じ数の原子どうしは化学的性質がよく似ている。」 とありますが,なぜそうなるのですか? また,具体的にはどのような例がありますか?



Http Www E Net Nara Jp Hs Gojo Index Cfm 1 1063 C Html 1063 Pdf



化学講座 第3回 元素の周期表 私立 国公立大学医学部に入ろう ドットコム
Nov 16, 17化学において「価電子」とは、最外殻の電子殻に存在する電子です。 原子が取り得る化学結合の種類は、価電子数によって決まるため、原子の価電子数の求め方を理解することは、価電子 は満席(希ガス配置)の芸術点にどれだけ近いかを表す! 原子は常に満席になりたがるので、 価電子が原子の性質を決める ! 最外殻電子とは、見晴らしの悪い部屋に入った電子も含める!Apr 24, 17価電子 とは、 最も 外側の殻の 4個の部屋に入っている電子の数;




パラジウムの価電子数って0でいいんでしょうか Peing 質問箱




原子価の意味と一覧 価電子 価標の違い Vicolla Magazine
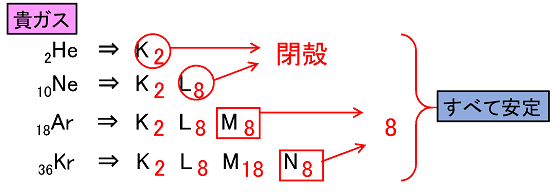
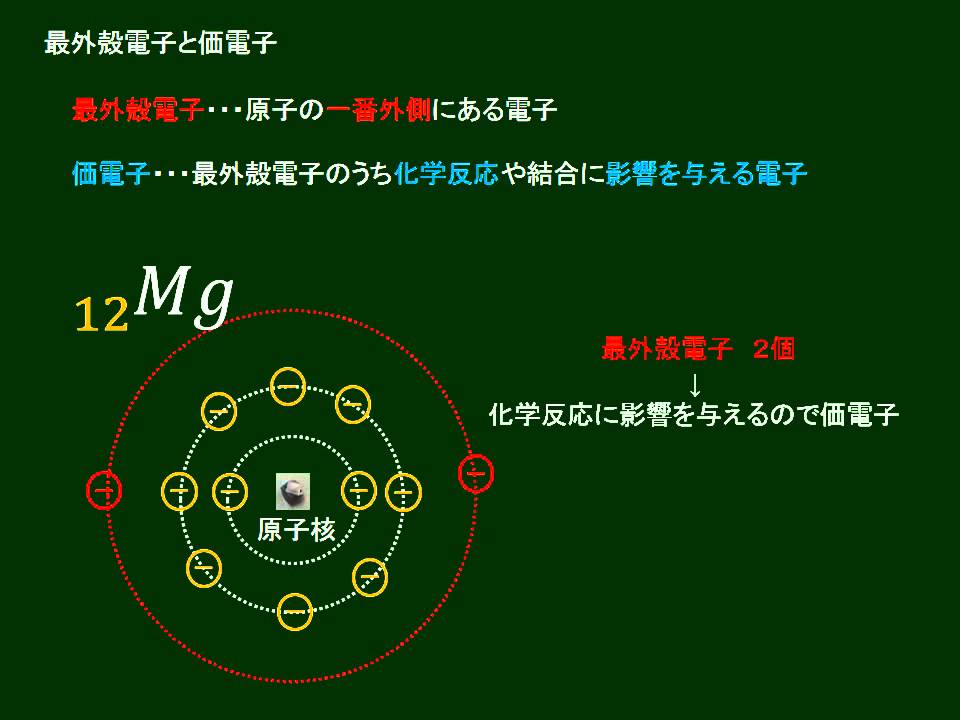
Jul 13, あいつらは一番外の電子殻(最外殻)に収容されている電子の数が2n²のマックスなので,閉殻構造を取っています。 そのため非常に安定で他の物質と反応しない『貴ガス』と呼ばれています。 アルゴンArも『貴ガス』の一種ですが,こいつは閉殻構造はナトリウムは最外殻に1個あった電子を放出し,ひとつ内側の電子8個のL殻が最外殻と なって安定化し,1価の陽イオンであるナトリウムイオン Na になりました。 今度は 12 Mg を考えましょう。電子配置は K2,L8,M2 です ね。 今度は最外殻に2個,ひとつ内側のL電子が収容されている最も外側の電子殻を最外殻といい tそこに含まれる電子を最外殻電子 または価電子という以下に各選択肢のルイス構造式を示す 1 ×:メチルアニオンの構造である炭素原子の最外殻に収容されている電子数は 8である u




高校理論化学 原子の電子配置 受験の月



シリコン原子の構造 太陽光発電の仕組み
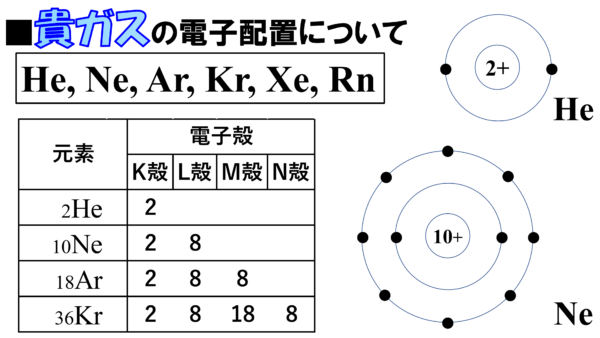
周期表と電子配置 イオンの生成 多くの原子は,不安定で単独では存在できない。 安定な原子は,最外殻の電子数が8個(価電子0)の貴ガス元素だけである。 そこで不安定な原子は安定化するため,最外殻の電子(-の粒子)を放出したり,受け取っ価電子が s 軌道と p 軌道に入っている原子の場合、最外殻の s 軌道と p 軌道(3個)を合わせた4個の軌道から分子軌道を作って、そこに全部2個ずつ電子が入った状態が、最も安定な状態になる(ことが多い つまり、最外殻電子は8個とは限りません。希ガス 価電子数 , 最外殻にある電子である価電子は、原子のイオンになりやすさや他の原子との結びつきやすさなどの化学的性質に大きく関係しています。希ガスはどういう電子配置をしているのか?化学を学んでいく上で重要なところです?



1 4 電子殻と電子配置 おのれー Note



価電子とは 数え方や覚え方 最外殻電子との違いは
Sep 14, 18なので、大抵の場合は 最外殻電子=価電子 です。 このように炭素の場合は、最外殻電子数と価電子数が同じく4個です。 カルシウムは、このように最外殻電子数2個で価電子数が2個で同数です。 最外殻電子と価電子に違いが出るときは?Oct 16, 13原子が化学結合をするとき、一番外側の電子殻にある電子が関係するので、「一番外側にあって化学結合に関係する電子の数」を「価電子数」といいます。 以上から分かるように、たいていの原子では 最外殻電子数=価電子数 となります。Nov 21, 価電子 価電子の概要 ナビゲーションに移動検索に移動基本的に、価電子数は最外殻電子数と等しい。また、典型元素(貴ガスを除く)は各族番号の1の位が価電子数となる。ただし、最外殻電子がちょうどその電子殻の最大収容数の場合、また




電子の基礎 1 電子とは 電気なんか嫌いだのブログ



Caの価電子数で 一般にk殻 2 L殻 8 M殻 18となってい Yahoo 知恵袋
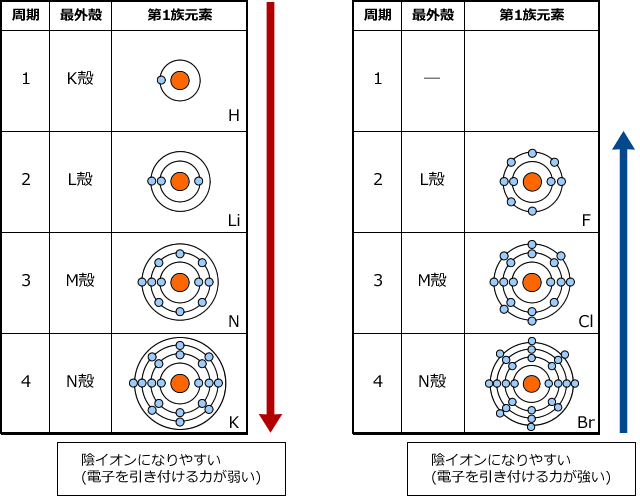
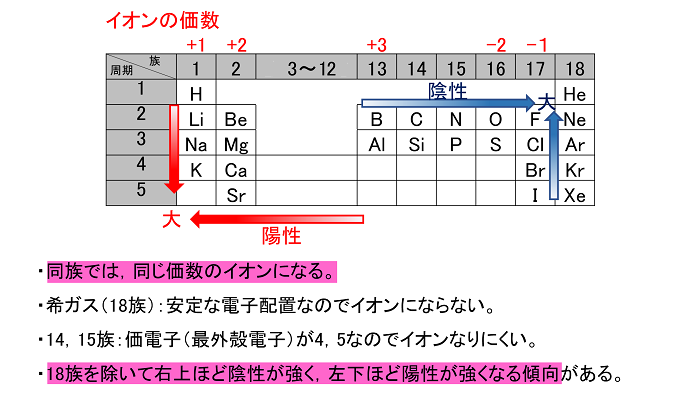
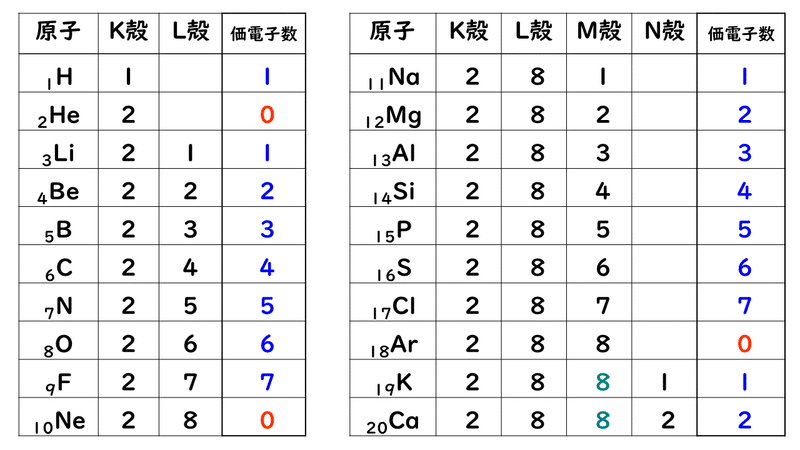
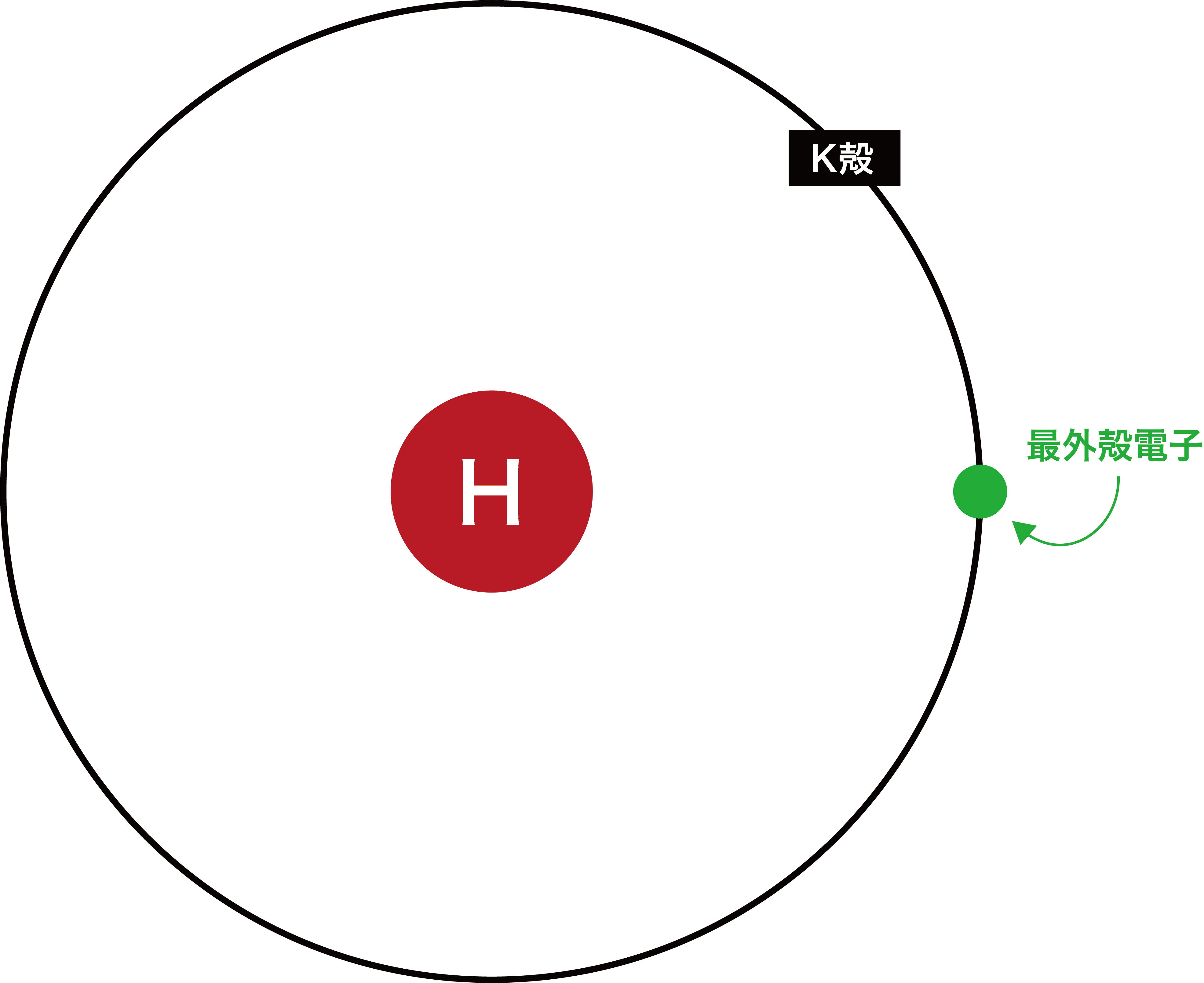
最外殻の電子(価電子)数が〔 1 ~ 3 〕個の原子は,最外殻の電子を放出して安定な電子配置となる。 電子を放出した分だけ正の電荷をもつ 。 名称は「~イオン」とつける 。 生成したイオンの電子配置は,原子番号の最も近い希ガス元素と同じになる 。基本的に、価電子数は最外殻電子数と等しい。 また、 典型元素 (貴ガス を除く)は各族番号の1の位が価電子数となる。 ただし、最外殻電子がちょうどその電子殻の最大収容数の場合、または最外殻電子が8個の場合、価電子の数は0とする。Apr 19, 16価電子の数 価電子は最外殻電子といっても良いです。 ただし、後で説明しますが希ガスは最外殻電子は安定しているので価電子とは数えません。 価電子の数を例で見てみましょう。 水素 \( _1 \mathrm H\) はK殻に1個の電子があり、価電子数は1です。



化学の問題ですバナジウム原子の最外殻電子の数はなぜ2個なのでし Yahoo 知恵袋
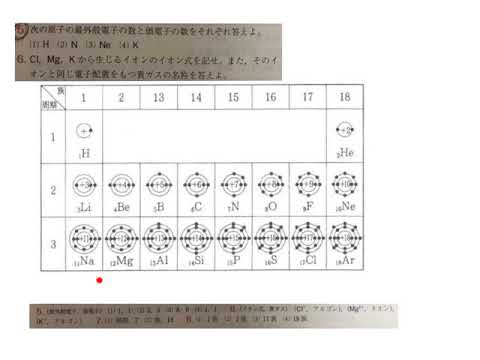



化学 最外殻電子と価電子 イオン Youtube
May 21, 最も外側の電子の数は「最外殻電子数」 最外殻電子数が一緒だと原子の性質が似る;



周期表とその見方 戻る 性質のよく似た元素が縦の列に並ぶように整理した表を周期表といいいます 元素の整理 族と周期 同族元素 電子の配置と価電子 価電子とは 最外殻電子の数 4 7 価電子の数 4 7 価電子 最外殻にある1から7個の電子 内側からn
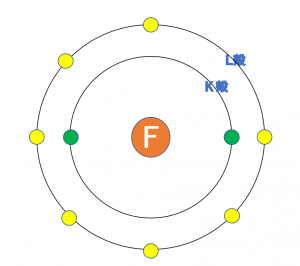



原子構造と電子配置 価電子 理系ラボ



1 6 元素の周期律と周期表 おのれー Note
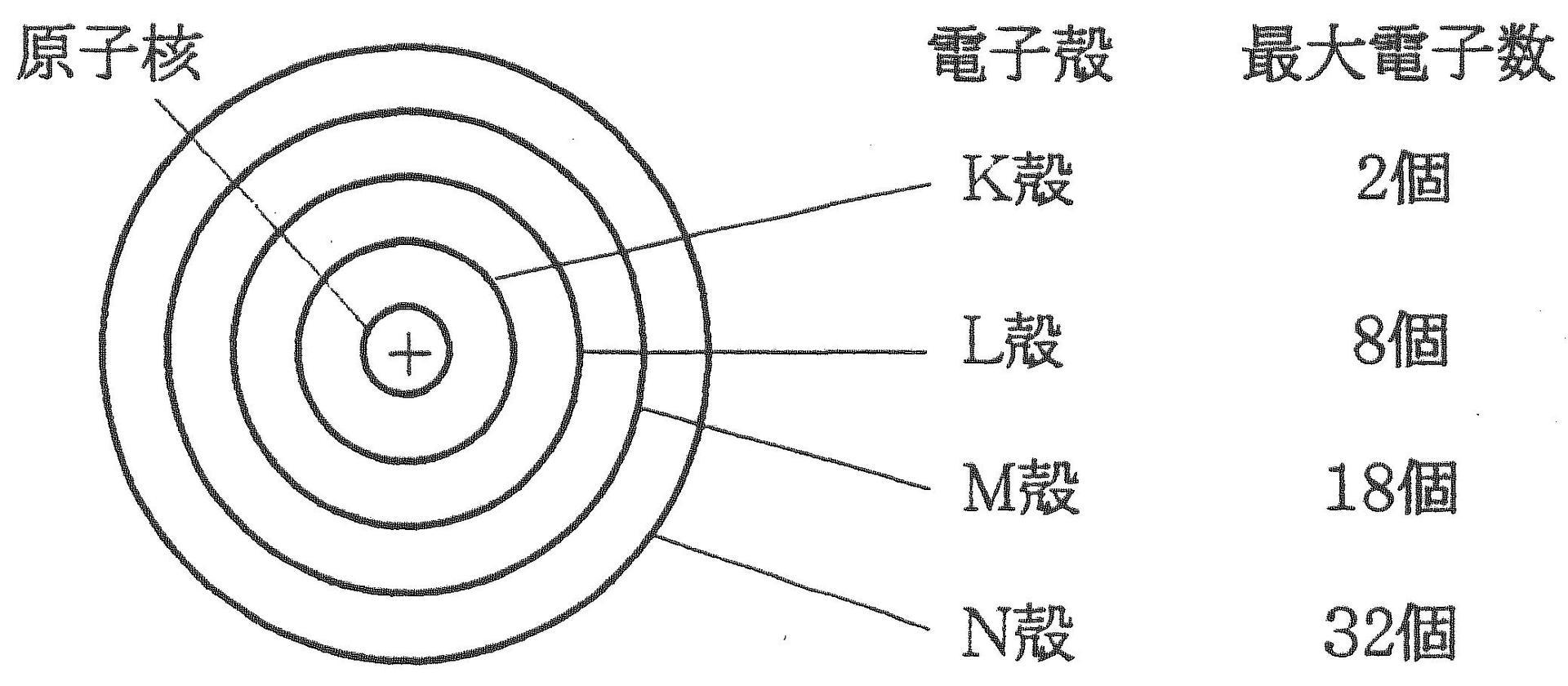



理論 電子配置と電子軌道 受験 定期テストで高校化学を完全攻略




受験生 高校生必見 周期表の覚え方 スイヘーリーベだけじゃナンセンス めんまのつぶやき




5分でわかる オクテット則 価電子のルールを理系ライターがわかりやすく解説 ページ 3 4 Study Z ドラゴン桜と学ぶwebマガジン
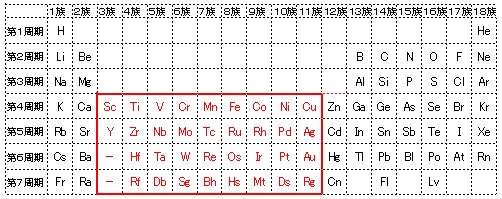



遷移元素の特徴とは 具体的な元素名と性質




共有結合を即理解 わかりやすい図で解説 高校生向け受験応援メディア 受験のミカタ




どうしてk カリウム の最外殻電子の数は1になるのですか 教えてください Clear



最外殻電子と価電子 違い 一覧 8個の理由など 化学のグルメ




高校化学 電子配置 最外殻電子 オンライン無料塾 ターンナップ Youtube




22 Square 1 4 D Descubre Como Resolverlo En Qanda



原子とイオン



1



3



最外殻電子と価電子 違い 一覧 8個の理由など 化学のグルメ




遷移元素の特徴 遷移元素のk殻 l殻 m殻 化学 By 藤山不二雄 マナペディア




最外殻電子と価電子の違いは 化学受験テクニック塾




未知なる人間 遥かなる宇宙 Twitter वर 最外殻電子数と価電子数 最外殻電子数とは 単純に最外殻にある電子数です 価電子 とは 反応に関与する電子数です 下図は価電子のグラフです 最外殻電子数のグラフとの違いを考えて下さい T Co



周期表とその見方 戻る 性質のよく似た元素が縦の列に並ぶように整理した表を周期表といいいます 元素の整理 族と周期 同族元素 電子の配置と価電子 価電子とは 最外殻電子の数 4 7 価電子の数 4 7 価電子 最外殻にある1から7個の電子 内側からn




図解 最外殻電子と価電子の定義と違い 結論 希ガスで異なります サイエンスストック 高校化学をアニメーションで理解する



Www Zkai Co Jp Wp Content Uploads Sites 15 19 09 Qcs5a1z1a2 Pdf



周期律と周期表 覚書
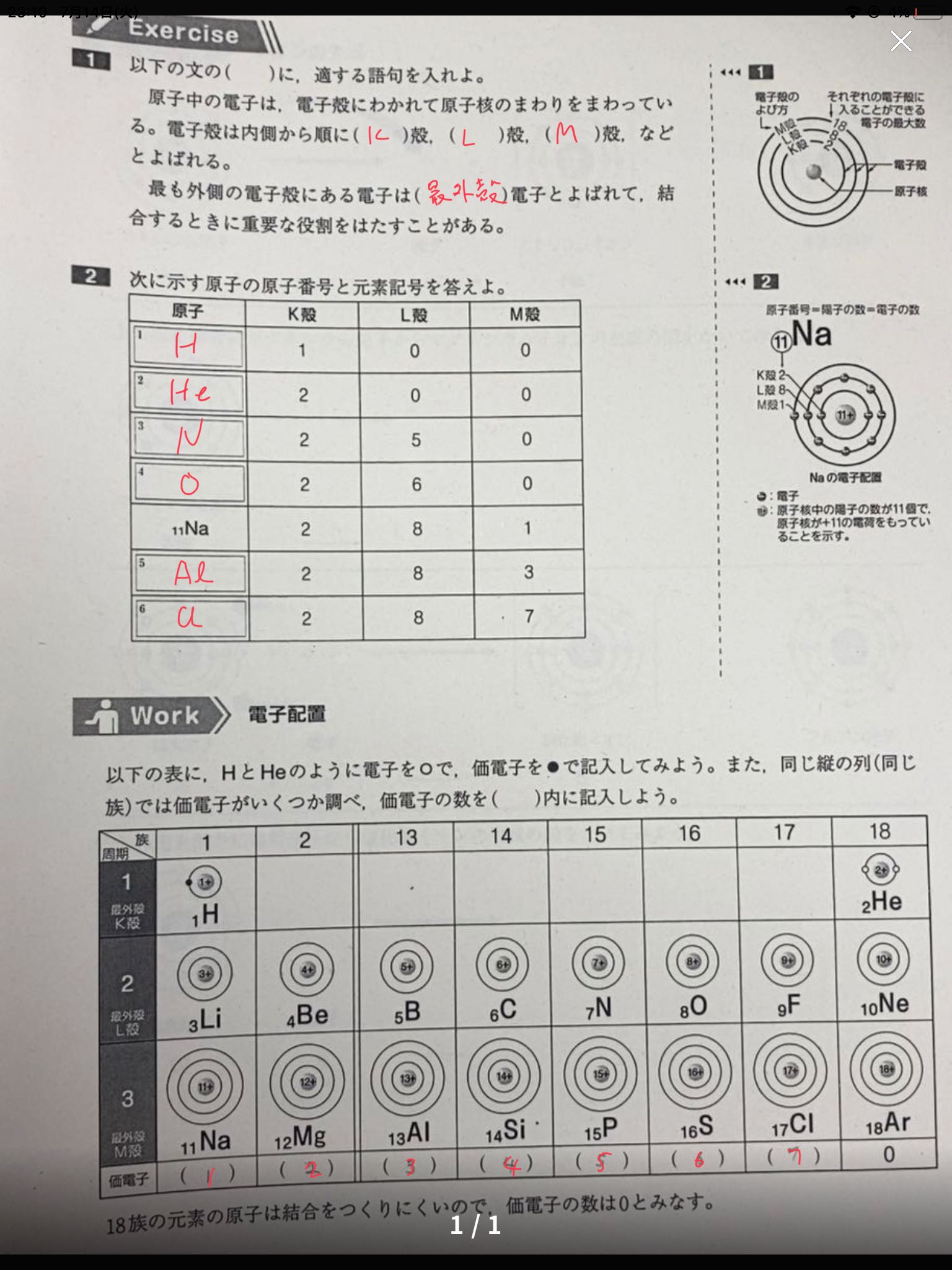



Exercise 33 1 1e See How To Solve It At Qanda




最外殻電子と価電子



受験基礎化学 6 電子配置 みかみの参考書ブログ




Descubre Como Resolverlo En Qanda




5分でわかる オクテット則 価電子のルールを理系ライターがわかりやすく解説 ページ 3 4 Study Z ドラゴン桜と学ぶwebマガジン




高校化学基礎 価電子とは 映像授業のtry It トライイット




内側からn番目の電子殻には 最大2nの二乗個の電子まで入るとありますが K殻は2個 Clear




右下の赤枠は 18族は安定になっているから価電子数が0 って意味で合ってますか Clear




イオン化エネルギー 電子親和力 電気陰性度のグラフの違いを区別せよ 化学受験テクニック塾




オクテット則 8電子則 大学化学講座



Q Tbn And9gcsehw5cwcaw6di4o3vedvsm7lzfqsols7n4fsxrmqq C2oljibh Usqp Cau




3 Ac Descubre Como Resolverlo En Qanda



教養の化学 第5週 13年10月21日 担当 杉本昭子 Ppt Download
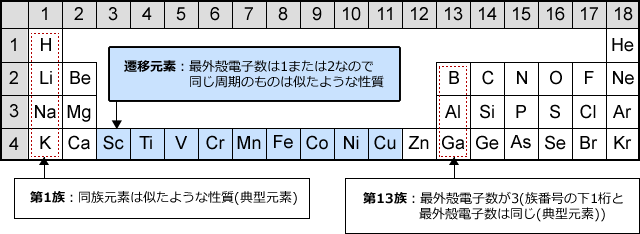



化学講座 第3回 元素の周期表 私立 国公立大学医学部に入ろう ドットコム




最外殻電子と価電子
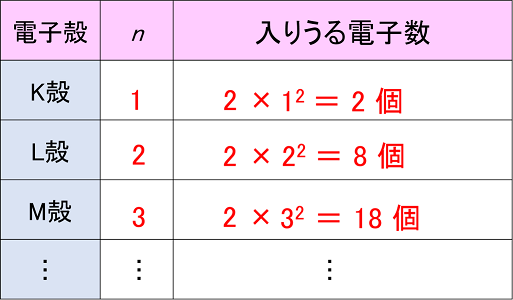



原子とイオン




原子価とは 原子価の求め方までわかりやすく解説 高校生向け受験応援メディア 受験のミカタ




オクテット則 8電子則 大学化学講座




最外殻電子と価電子の違いは 化学受験テクニック塾



化学基礎 最外殻電子と価電子 Youtube




原子価とは 原子価の求め方までわかりやすく解説 高校生向け受験応援メディア 受験のミカタ



共有結合と価電子 理科の講義ノート Lecture Notebook



なんとなくわかる高校化学 価電子



図解 最外殻電子と価電子の定義と違い 結論 希ガスで異なります サイエンスストック 高校化学をアニメーションで理解する



イオン



Qck0d2a9as2853cudbqy0lc6cfz4a0e7e Xyz Kiso Electrons In The Outermost Shell



Q Tbn And9gcsehw5cwcaw6di4o3vedvsm7lzfqsols7n4fsxrmqq C2oljibh Usqp Cau



危険物資格取得のための高校化学no 6 電子殻と電子配置 F M サイエンスブログ



図解 最外殻電子と価電子の定義と違い 結論 希ガスで異なります サイエンスストック 高校化学をアニメーションで理解する



1 4 電子殻と電子配置 おのれー Note



化学重要問題集8 11 原子 イオン Tekibo




最外殻電子と価電子




希ガスの電子配置は価電子ゼロの閉殻であっていますか Clear




高校化学基礎 周期律と価電子 映像授業のtry It トライイット




高校化学基礎 周期律と価電子 映像授業のtry It トライイット




原子 自立学習塾 Potergy ポテジー



なんとなくわかる高校化学 価電子



最外殻電子と価電子 違い 一覧 8個の理由など 化学のグルメ
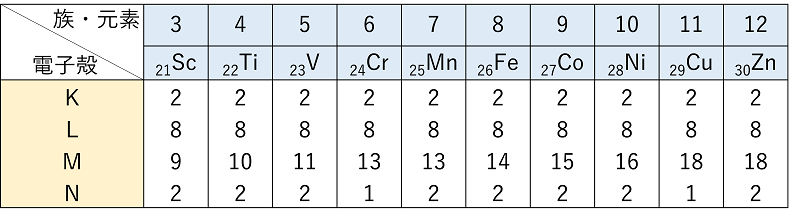



遷移元素の特色



イオン 化学コラム
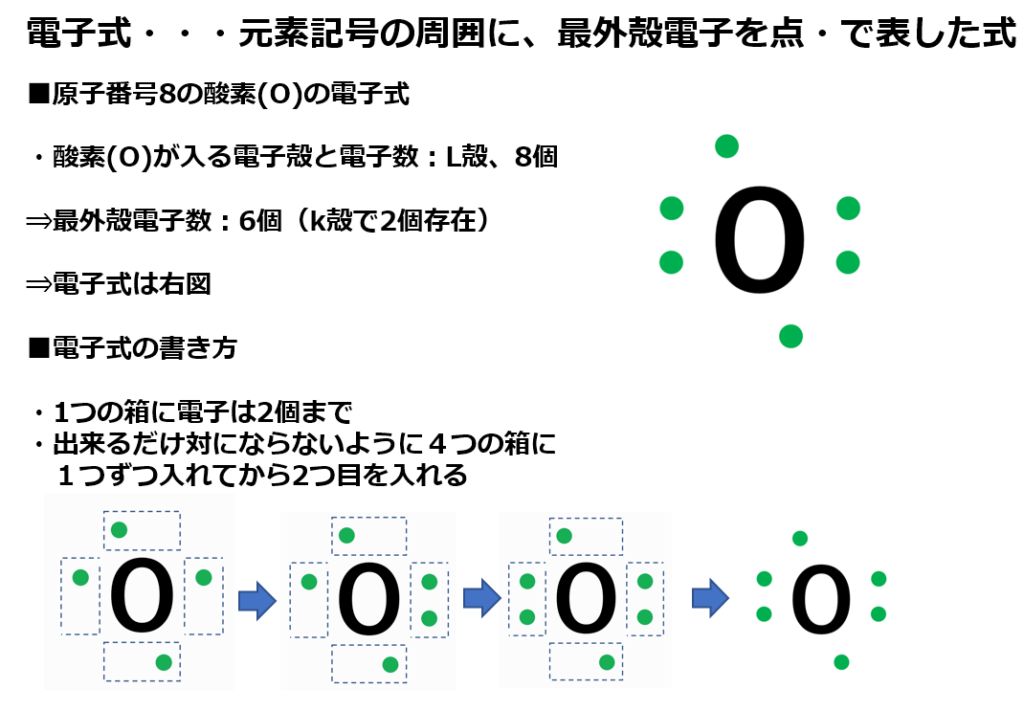



酸化還元反応 電子のやり取り




最外殻電子と価電子の違いは 化学受験テクニック塾
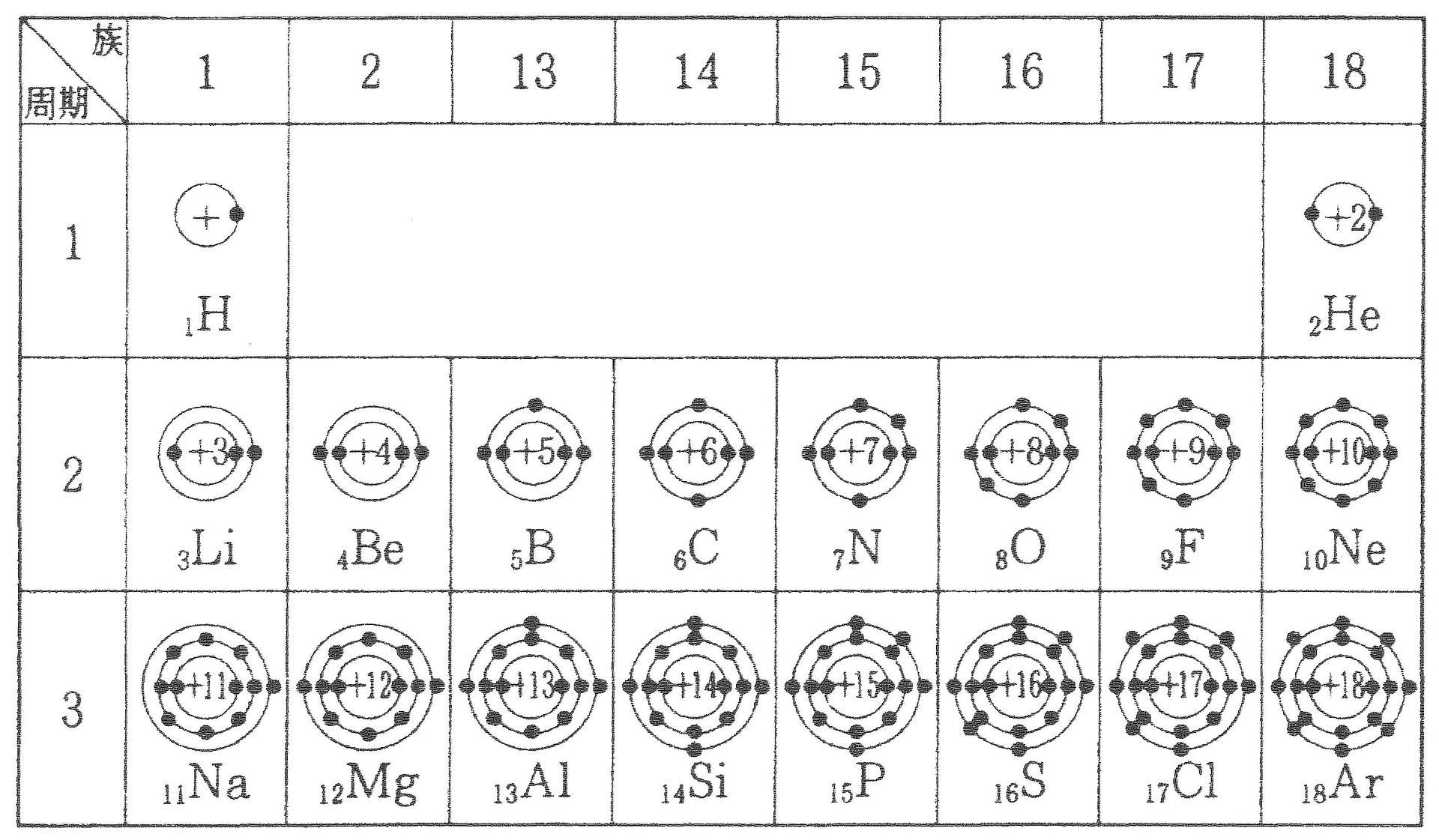



理論 電子配置と電子軌道 受験 定期テストで高校化学を完全攻略



価電子 Chemihack おうちで学べる化学
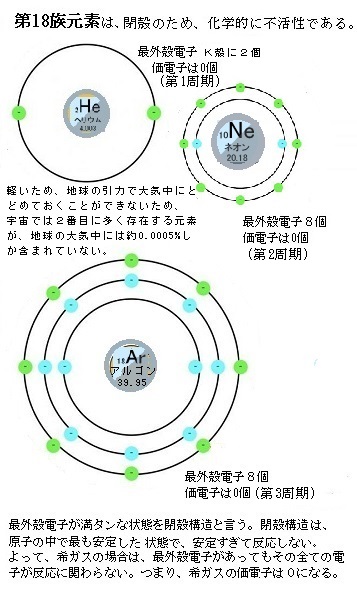



車山高原レア メモリーが語る 元素の周期表



受験基礎化学 6 電子配置 みかみの参考書ブログ




高校化学基礎 原子価とは 映像授業のtry It トライイット




5分でわかる 陽イオン 陰イオン 単原子イオン の価数の考え方と覚え方 電子配置を図で解説 サイエンスストック 高校化学をアニメーションで理解する




なぜヘリウムは電子の数か2個なのに価電子は0個なんですか なぜヘリ 高校 教えて Goo




価電子数と最外殻電子数 高校物理 高校化学家庭教師 ズバリ教えます



1 4 電子殻と電子配置 おのれー Note



1 4 電子殻と電子配置 おのれー Note



化学講座 第4回 第一イオン化エネルギーと第nイオン化エネルギー 私立 国公立大学医学部に入ろう ドットコム




価電子 Chemihack おうちで学べる化学



希ガスの価電子の数が0であり 最外殻電子の数と違う理由



2 1 価電子と化学結合 スペクトル色々




至急です Clの価電子は7なので 陰イオンになりますが M殻は電子18 化学 教えて Goo
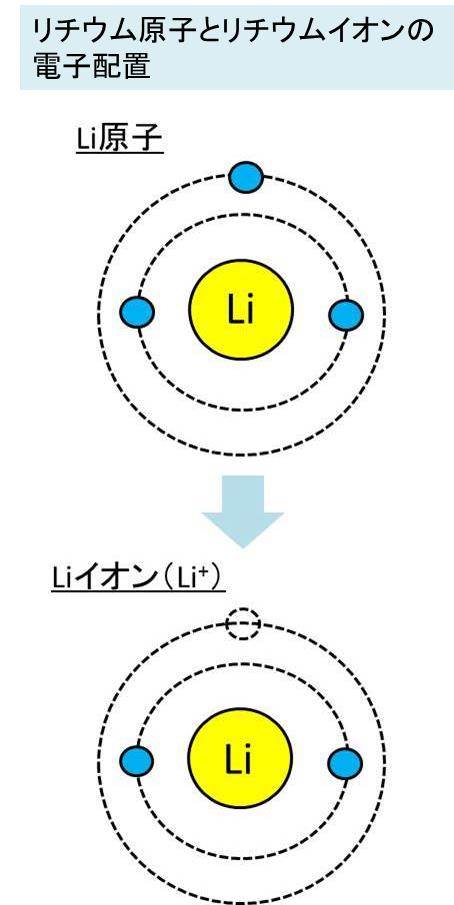



価電子とは 数え方や覚え方 最外殻電子との違いは




最外殻電子と価電子




高校化学基礎 希ガスの電子配置 映像授業のtry It トライイット
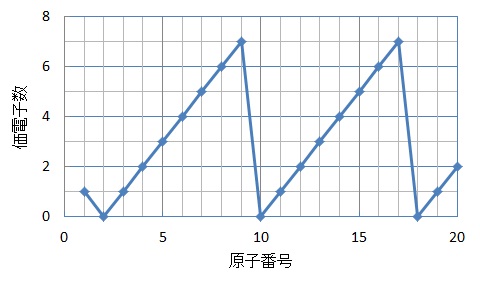



周期表 化学基礎 高校化学net参考書




価電子とは 価電子数の数え方をやさしく説明するよ 授業 レベルa2 ともよし塾 受験と科学の解説授業




オクテット則 8電子則 大学化学講座



塩素 Cl の最外殻電子の数について 塩素は原子番号が17なので K殻 Yahoo 知恵袋




ヘリウムの最外殻電子の数って8個ではないんですか Clear


コメント
コメントを投稿